¿podríamos ver el fin de las inyecciones de insulina?
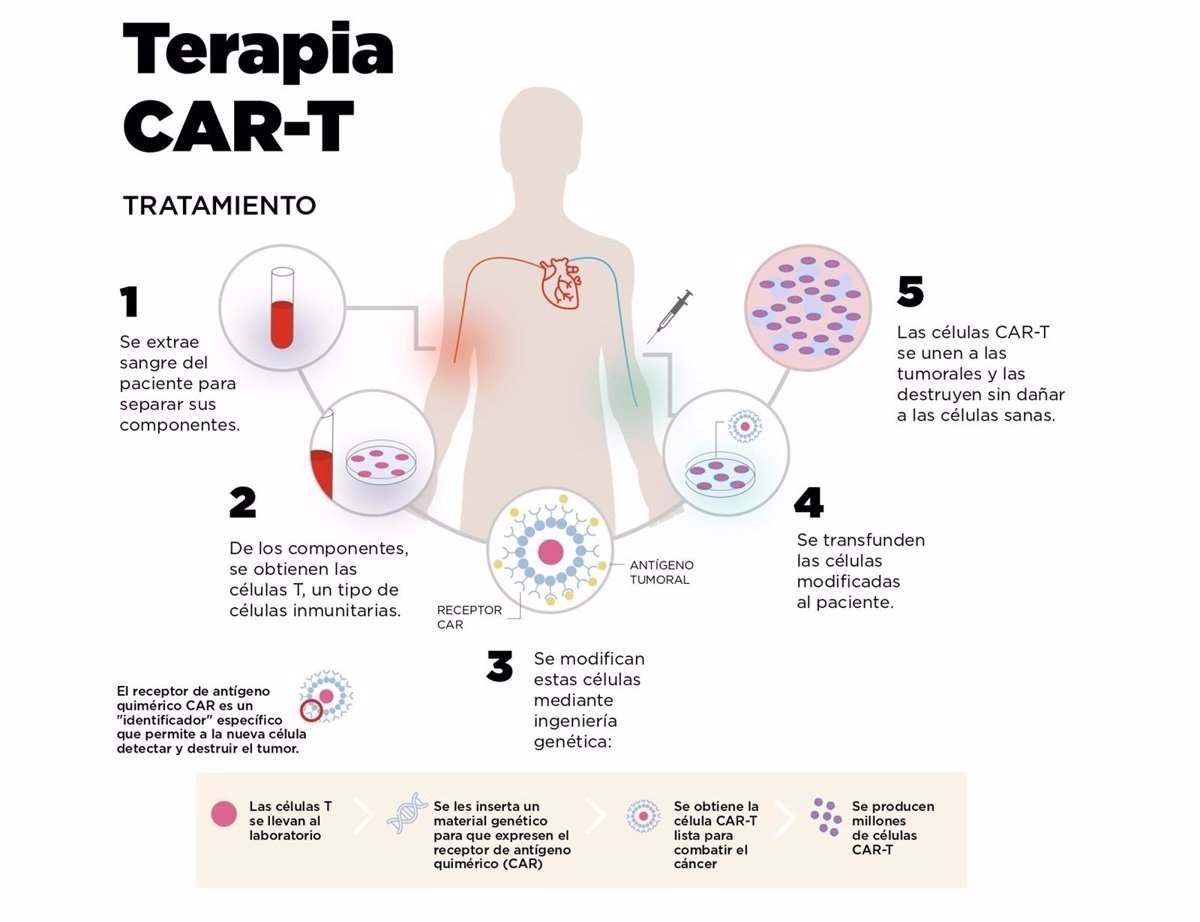
Se trata de células del sistema inmune, conocidas como linfocitos T, que son modificadas genéticamente para reconocer un antígeno específico. En el caso de los cánceres hematológicos, se trata de células T citotóxicas, que reconocen la célula tumoral y la destruyen. En la diabetes, en cambio, se centran en las reguladoras de la inflamación.
La diabetes es una incapacidad de regular la presencia de glucosa en sangre relacionada con un problema para el procesamiento de la insulina. En el caso de la diabetes tipo 2, la más frecuente, es resultado casi siempre del estilo de vida (obesidad, sedentarismo), que acaba generando una resistencia a la insulina, vital para procesar la glucosa presente en la sangre y que entre en las células.
La diabetes tipo 1, en cambio, es una enfermedad autoinmune provocada por la destrucción de las células beta del páncreas, las productoras de insulina, a través de los linfocitos T. Supone entre el 1% y el 5% de todos los casos de diabetes, unas 90.000 personas en España según la Sociedad Española de Diabetes.
Suele diagnosticarse a edades tempranas (4,9 años cuando se detecta en la infancia) y el 50% de los pacientes presenta otras patologías asociadas, desde la alteración de los niveles de colesterol hasta retinopatías y nefropatías. Aunque no está relacionada con el estilo de vida, este sí que afecta al desarrollo de la enfermedad.
El equipo del argentino Juan Carlos Jaume, profesor de Endocrinología de la Universidad de Toledo (Ohio, Estados Unidos), obtuvo muestras de sangre y de páncreas de pacientes a los que se le extrajo por alguna razón clínica (cáncer de páncreas y pancreatitis). De la sangre obtuvieron células T reguladoras, abreviadas como Tregs, que se encargan de regular o suprimir a otras células del sistema inmunitario, las cultivaron y las modificaron genéticamente para reconocer antígenos relacionados con las células beta.
Con esta modificación introdujeron otra: asociaron a los linfocitos T editados (CAR Tregs) una proteína fluorescente verde. De esta forma podían verificar si las células, cuando se introdujeran en los islotes de Langerhans (las estructuras del páncreas que producen las células beta), sobrevivían y proliferaban.
Los investigadores cultivaron los islotes pancreáticos obtenidos de los páncreas humanos y los combinaron con las CAR Tregs, que proliferaron en las siguientes 72 horas. También los probaron en ratones modificados para expresar la diabetes tipo 1 humana, mostrando el mismo comportamiento: estos linfocitos, modificados genéticamente, suprimían la respuesta de los linfocitos T citotóxicos que atacan a las células beta del páncreas, regenerando la producción de insulina en el cuerpo.
La revolución de las CART
«Este es el siguiente paso de las células CAR», explica el presidente de la Sociedad Española de Inmunología, Marcos López Hoyos. «Primero han sido las neoplasias (cánceres) hematológicas y, en un plazo relativamente corto, se emplearán en tumores de órgano sólido. Las enfermedades autoinmunes [como la diabetes tipo 1] son las siguientes».
De hecho, ya hay ensayos «en fases tempranas» para el lupus o la esclerosis múltiple, y también para evitar el rechazo en trasplantes de órgano sólido. «El concepto de célula T reguladora estuvo de moda en los años 80 entre inmunólogos», recuerda, «pero cayeron en desuso y estaban hasta proscritas», debido a la dificultad para caracterizarlas molecularmente.
En cambio, las células T efectoras, las que destruyen células, tuvieron mayor éxito. «Podemos eliminar con células todo lo que estamos eliminando con anticuerpos monoclonales», terapias que han supuesto un paso adelante en el tratamiento del cáncer en las dos últimas décadas.
Con todo, López Hoyos no cree que, si supera todos los ensayos clínicos en humanos necesarios para ser aprobada, esta terapia se vaya a utilizar mucho en diabetes tipo 1, una enfermedad bien controlada en la actualidad gracias a las innovaciones en la administración de insulina, que la hacen cada vez más cómoda para los pacientes.
«Pueder ser una vía de tratamiento, sobre todo, en casos considerados rebeldes», opina el inmunólogo. Sin embargo, el estudio es un paso más para demostrar el potencial de una nueva vía para tratar numerosas enfermedades.
«Esta terapia está en sus inicios», comenta. «Las CAR se han desarrollado porque, metodológicamente, hemos aplicado multitud de herramientas moleculares y porque en los últimos 20 años hemos aprendido cantidad de mecanismos de respuesta inmunitaria que no conocíamos antes». Por eso, «en los próximos 20 años el cambio será espectacular».
(image)
Este post se basa en el tema «¿podríamos ver el fin de las inyecciones de insulina?« publicado en Diabetes Foro.
Puedes ver los comentarios de los miembros del foro y hacer los tuyos en «¿podríamos ver el fin de las inyecciones de insulina?«