La empresa biofarmacéutica Prevention Bio fue fundada en 2016 por Francisco León ?de la que actualmente es director científico ejecutivo?y Ashleigh Palmer ?actual consejero delegado?. El laboratorio se dedica a interceptar y a prevenir enfermedades autoinmunes, entre las que se encuentran también la enfermedad celíaca y la miocarditis.
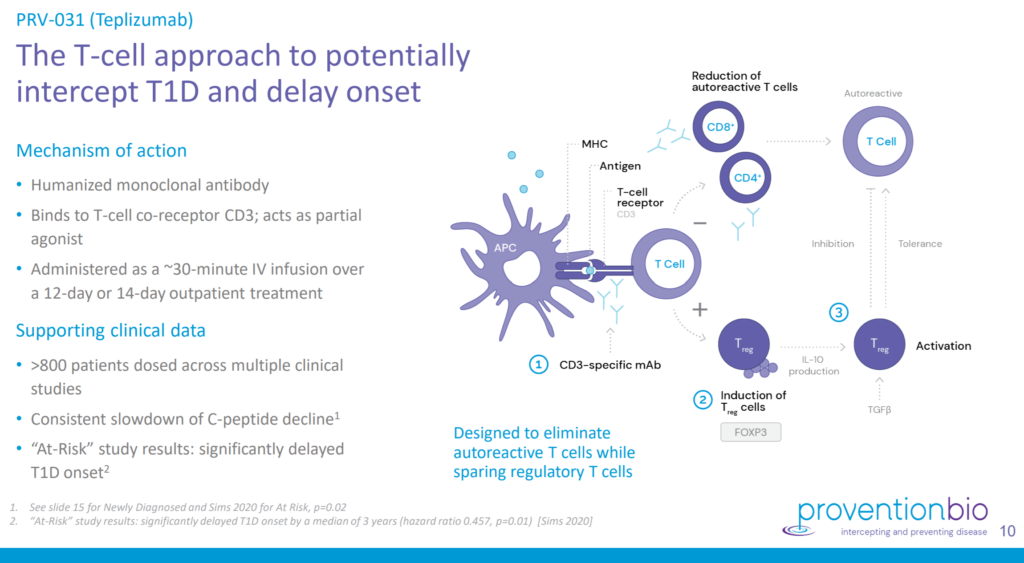
El anticuerpo monoclonal Teplizumab, que se comercializará bajo la marca Tzield, de Provention Bio y Sanofi, es una vacuna que se administra de forma intravenosa. El medicamento dirige al sistema inmunológico sus propias células productoras de insulina.
De momento, la terapia se comercializará en Estados Unidos, aunque Francisco León espera que pronto llegue a la sanidad española. «Estamos estudiando la mejor forma de traerlo a Europa y España, sin fecha concreta pero cuanto antes mejor», asegura desde Nueva Jersey.
El esfuerzo
«Es una satisfacción ver que podemos ayudar a evitar una enfermedad a miles de personas»
Para este emprendedor leonés «es una satisfacción enorme ver que podemos por fin ayudar a evitar una enfermedad autoimmune crónica a miles de personas».
En los ensayos clínicos, Tzield retrasó la progresión a la diabetes en un poco más de dos años. Según informa la compañía, los beneficios han durado mucho más en algunos de los participantes del estudio.
La cadena de noticias CNN ha divulgado en Estados Unidos la información tras la aprobación de la FDA con el testimonio de varias personas participantes en los ensayos clínicos. Una de ellas, Mikayla Olsten, fue examinada para detectar diabetes después de que su hermana Mia, de 9 años, desarrollara repentinamente un episodio potencialmente mortal de cetoacidosis diabética y le diagnosticaran diabetes.
No había antecedentes de diabetes en la familia y Mikayla no estaba enferma, pero tenía cuatro de los cinco tipos de autoanticuerpos que los médicos buscan para evaluar el riesgo de una persona. «Nos dijeron que cuando alguien tiene tantos marcadores, la duda no es si va a desarrollar diabetes, sino cuándo», dijo su madre, Tracy. Mikayla tenía 15 años cuando se unió al estudio y recibió teplizumab. Ahora tiene 21 años y está en el último año de la universidad. Se somete a una serie de pruebas anuales para revisar su páncreas y marcadores sanguíneos, y Tracy Olsten dice que su diabetes no ha progresado en seis años.
Llegada a Europa
«Estamos estudiando la mejor forma de traerlo a Europa y España, cuanto antes mejor»
Según una investigación de la Endocrine Society y la American Diabetes Association, cuando una persona tiene marcadores de enfermedad autoinmune y episodios de azúcar en sangre descontrolada, el riesgo de cinco años de progresión a una enfermedad sintomática insulinodependiente es del 75 %. El riesgo de por vida de desarrollar diabetes insulinodependiente es casi del 100%.
«Esta es una ocasión histórica para la comunidad de diabetes tipo 1 y un cambio de paradigma. para personas de 8 años o más en etapa 2 que ahora tienen una terapia aprobada por la FDA para retrasar la aparición de la enfermedad en etapa 3, un retraso en el inicio de la etapa 3 que da perspectiva al paciente y la familia; más tiempo para vivir sin diabetes», señala Ashleigh Palmer, cofundador y director ejecutivo de Prevention Bio.
El principal desafío al recetar Tzield será encontrar personas que lo necesiten. El medicamento está aprobado para personas que no tienen ningún síntoma de la enfermedad y es posible que no sepan que están en camino de contraerla. «La detección se convierte en un problema realmente importante, porque lo que sabemos es que alrededor del 85% de los diagnósticos de tipo 1 en la actualidad se encuentran en familias que no tienen antecedentes familiares conocidos».
El uso
Tzield está aprobado para su uso en personas mayores de 8 años que se encuentran en la etapa 2 de su diabetes tipo 1. En esa etapa, los médicos pueden medir los anticuerpos que atacan las células beta productoras de insulina en la sangre de la persona, y tienen niveles anormales de azúcar en la sangre, pero su cuerpo aún puede producir insulina.
«La forma en que no solo la industria, sino también nuestro sistema médico manejan las enfermedades autoinmunes, y especialmente la diabetes tipo 1, es realmente subóptima en la época actual», asegura Ashleigh Palmer.
En octubre de 2022, la empresa anunció un acuerdo de copromoción para el lanzamiento en EE UU de Tzield. Los responsable de Sanofi consideran que esta aprobación es una «victoria profunda y largamente esperada para la comunidad diabética» y agraceden a Provention Bio «por su inquebrantable determinación de llevar a los pacientes la primera terapia modificadora de la enfermedad. Esperamos aprovechar la infraestructura y la experiencia de Sanofi para ayudar a las personas en lo necesitan en los EE UU».
Llegada a Europa
«Estamos estudiando la mejor forma de traerlo a Europa y España, cuanto antes mejor»
El tratamiento se administra una vez al día durante dos semanas. La inyección se suministra estéril, sin conservantes, transparente e incolora. Los efectos secundarios más comunes informados fueron glóbulos blancos y células linfáticas bajas, sarpullido y dolor de cabeza.
En los ensayos clínicos, el tratamiento ha detenido la enfermedad antes de que aparezcan los síntomas, al detener la destrucción de las células beta. El tratamiento reinicia el sistema inmunológico.
A diferencia de la diabetes tipo 2, que se puede prevenir con cambios en el estilo de vida, como perder peso y hacer ejercicio, la tipo 1 es una enfermedad genética que hasta ahora no ha tenido opciones de prevención. Hasta ahora.
El leonés participó en septiembre en León en el 43 Congreso de la Sociedad Española de Inmunología, que reunió a quinientos científico. Francisco León ha colaborado con el equipo del Hospital de León en ensayos sobre la enfermedad celíaca.
(image)
Este post se basa en el tema «La primera terapia contra la diabetes tipo 1« publicado en Diabetes Foro.
Puedes ver los comentarios de los miembros del foro y hacer los tuyos en «La primera terapia contra la diabetes tipo 1«